 手机访问:wap.265xx.com
手机访问:wap.265xx.com【中银医药】新冠口服药系列跟踪——阿兹夫定
炒股就看金麒麟分析师研报,权威,专业,及时,全面,助您挖掘潜力主题机会!
 分析师:邓周宇/联系人:薛源
分析师:邓周宇/联系人:薛源
6月30日国家药品监督管理局药品审评中心“上市药品信息”公示了真实生物阿兹夫定片的申请上市技术审评报告及说明书。NMPA官网信息显示阿兹夫定对《药品生产许可证》进行了变更,其生产厂家变更为河南真实生物科技有限公司、北京协和药厂有限公司两家,表明真实生物可委托其他药企生产阿兹夫定,而自身也已具备自行生产阿兹夫定的资质。
真实生物阿兹夫定HIV适应症获批,可能引起市场对新冠适应症上市的关注。国家药监局CDE在6月底公示了阿兹夫定片以HIV为适应症的申请上市技术审评报告和说明书,可能引发市场对于阿兹夫定以新型冠状病毒为适应症的获批的进一步关注。目前真实生物已经向NMPA递交了阿兹夫定的新药上市申请(NDA),目前正处于审评审批阶段,公司表示正争取尽快推进阿兹夫定作为治疗新冠肺炎药物上市。
阿兹夫定为国内新冠小分子药物进展较快的药物之一。国内外药企争相推动新冠小分子口服药研发和商业化进程,国外仍以辉瑞Paxlovid为首要推广药物,国内来看主要以真实生物的阿兹夫定、的VV116、开拓药业的普克鲁胺进展较快。近期公布的临床结果显示阿兹夫定具备较为显著的抗新冠病毒活性,对患者展示出良好的治疗效果,能较明显地缩短病人的核酸转阴时间、治疗时间和住院时间。目前阿兹夫定在中国、俄罗斯、巴西开展的针对中重度新冠患者的III期临床试验已完成,临床数据有待公布。
阿兹夫定生产开始布局,相关企业或将获益。真实生物已经先后与、、签订了针对阿兹夫定的委托生产协议,目的是为获批上市后的商业化生产做足准备,产品研发、产品生产以及市场推广布局已经开始铺开。此外,北京协和药厂和真实生物系阿兹夫定在国家药品监督管理局备案登记的生产厂家,真实生物拥有阿兹夫定的自主知识产权。
投资建议
国内在研的新冠小分子药物均还未获批,阿兹夫定作为研发进展较快的新冠口服药之一,值得关注。建议关注与真实生物展开生产合作的新华制药、华润双鹤、奥翔药业、。
医改政策波动风险,市场竞争加剧风险,上游原材料涨价风险。
阿兹夫定HIV适应症获批,新冠适应症上市推进中
2022年6月30日,国家药品监督管理局药品审评中心(CDE)“上市药品信息”公示了真实生物阿兹夫定片的申请上市技术审评报告和说明书。根据国家药监局官网的境内生产药品备案信息公示显示,6月29日,真实生物对阿兹夫定片进行了备案,阿兹夫定片生产企业由北京协和药厂变更为河南真实生物科技有限公司和北京协和药厂有限公司。此次公开的阿兹夫定片按照化药1类提交上市申请,用于治疗高病毒载量(HIV-1 RNA≥ 100000 copies/ml)的成年 HIV-1 感染患者。
 阿兹夫定(Azvudine)是由河南师范大学教授常俊标带队发明、郑州大学和河南省分析测试研究中心联合研制的药物,最初用于治疗艾滋病。由于阿兹夫定是新型核苷类逆转录酶和辅助蛋白Vif抑制剂,是全球首个上述双靶点抑制药物,为国内第一个拥有自主知识产权的抗艾滋病毒口服药物。它能够选择性进入HIV-1靶细胞外周血单核细胞中的CD4细胞或CD14细胞,发挥抑制病毒复制功能。2021年7月20日,国家药监局批准阿兹夫定片上市,用于治疗高病毒载量的成年HIV-1感染患者。目前新增临床试验为抗新型冠状病毒适应症,相关全球多中心III期临床试验已经完成,结果尚未公开发布。此外,根据Insight数据库披露,阿兹夫定针对丙型病毒肝炎的研发目前尚处于临床前试验阶段,靶点为非结构性蛋白5B。
阿兹夫定(Azvudine)是由河南师范大学教授常俊标带队发明、郑州大学和河南省分析测试研究中心联合研制的药物,最初用于治疗艾滋病。由于阿兹夫定是新型核苷类逆转录酶和辅助蛋白Vif抑制剂,是全球首个上述双靶点抑制药物,为国内第一个拥有自主知识产权的抗艾滋病毒口服药物。它能够选择性进入HIV-1靶细胞外周血单核细胞中的CD4细胞或CD14细胞,发挥抑制病毒复制功能。2021年7月20日,国家药监局批准阿兹夫定片上市,用于治疗高病毒载量的成年HIV-1感染患者。目前新增临床试验为抗新型冠状病毒适应症,相关全球多中心III期临床试验已经完成,结果尚未公开发布。此外,根据Insight数据库披露,阿兹夫定针对丙型病毒肝炎的研发目前尚处于临床前试验阶段,靶点为非结构性蛋白5B。

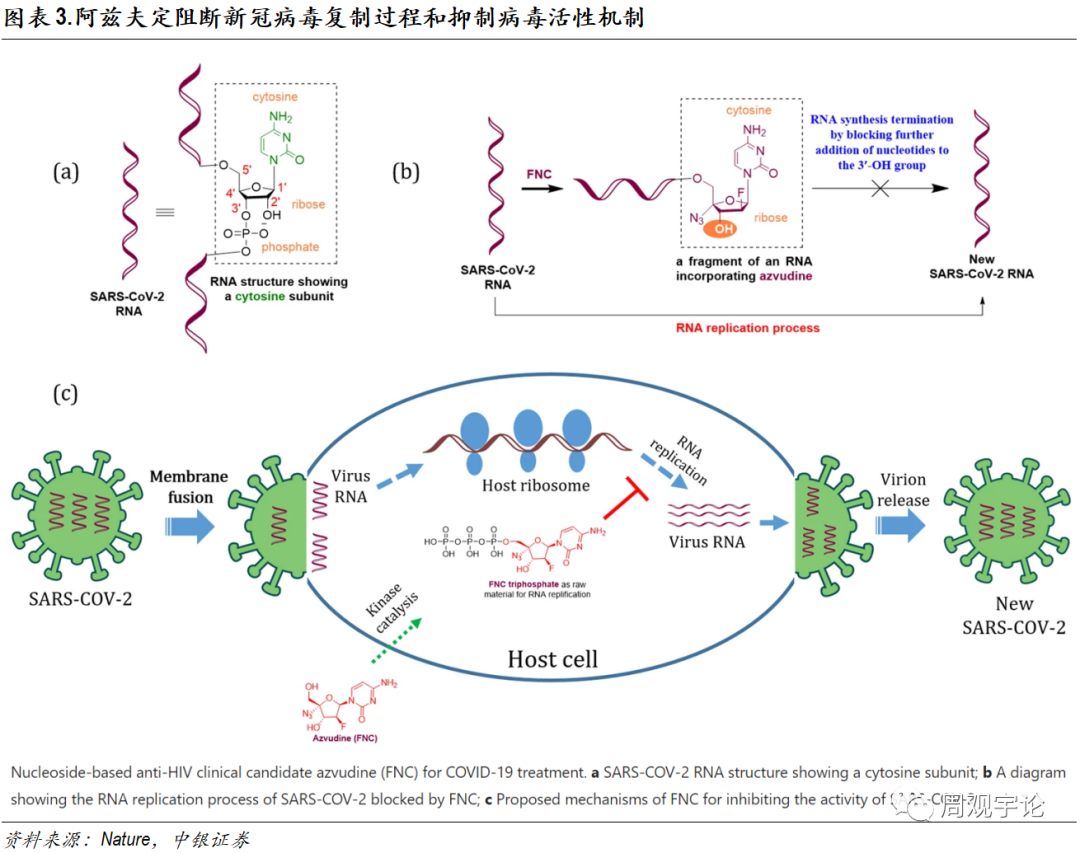
阿兹夫定针对新冠病毒的III期临床试验已结束,公司正积极推进上市进程中。阿兹夫定是一种通过阻断病毒 RNA 复制来抑制新冠病毒的RdRp抑制剂。2020年2月,阿兹夫定就被发现具有抗新冠病毒的作用,同年4月,阿兹夫定获国家食品药品监督管理局(SFDA)批准开启抗新冠病毒III期临床试验。2022年4月16日,中国医学发展大会上公开了阿兹夫定 II 期临床研究进展,新冠患者口服阿兹夫定后 3-4 天可以快速达到核酸转阴,平均用药时间为 6-7 天,平均出院时间为 9 天;重症与轻症治疗效果类似,且安全性良好。此前的体外研究结果披露,阿兹夫定的活性不如瑞德西韦,但是体内活性则优于瑞德西韦,原因在于只在胸腺完成三磷酸化,从化学治疗转化到免疫治疗,抗病毒同时保护了免疫系统。2022年4月21日,真实生物官方称根据初期临床试验,阿兹夫定显示出较为显著的抗新冠病毒活性,对患者展示出良好的治疗效果,能较明显缩短病人的核酸转阴时间、治疗时间和住院时间。此外,阿兹夫定每日仅需口服5mg,一个疗程为35mg,而瑞德西韦需要每日注射100mg。
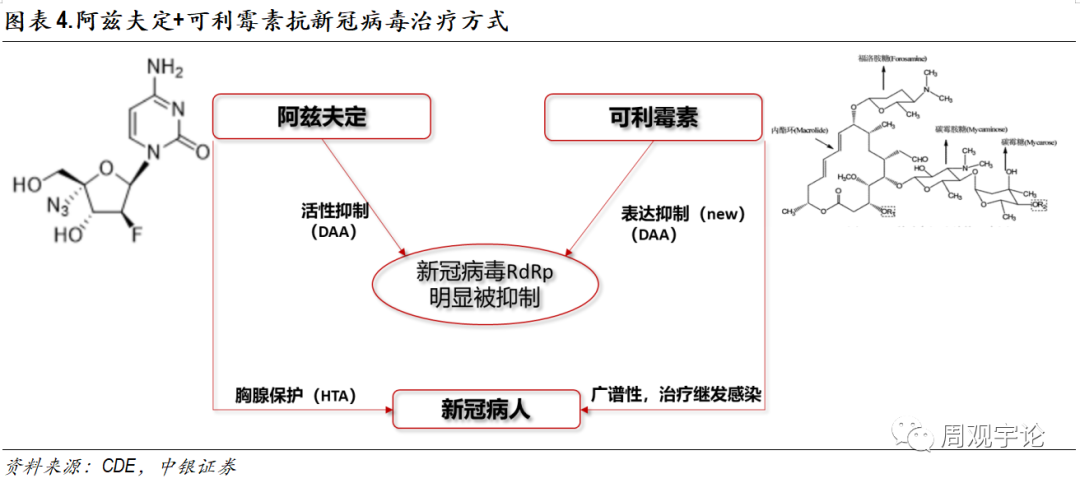
治疗方式上,中国工程院院士蒋建东建议采用阿兹夫定+可利霉素的A+B方案,可利霉素是世界上第一个利用合成生物技术研发、具有中国自主知识产权的1类创新药,对革兰氏阳性菌有较强的活性,尤其对肺炎链球菌、肺炎支原体、衣原体活性强,对红霉素和β-内酰胺类抗生素耐药菌、流感杆菌、军团菌、绿脓杆菌、产气荚膜梭菌有抗菌活性;与同类药没有完全交叉耐药性。它有较高的亲脂性,口服吸收快,组织渗透性强,分布广,体内维持时间长,有较好的抗生素后效应和免疫调节作用。阿兹夫定联合可利霉素配合用药,可以清除除新冠病毒外的其他感染,达到治疗双保险的效果。
 目前阿兹夫定在中国、俄罗斯、巴西开展的针对中重度新冠患者的III期临床试验已经完成,临床数据有待公布。目前真实生物已经向NMPA递交了阿兹夫定的新药上市申请(NDA),目前正处于审评审批阶段。根据国家药监局药审中心的信息披露,真实生物分别于今年3月10日、4月2日申请了II类和III类沟通交流会,当前状态为“已反馈”,目前公司正推进阿兹夫定治疗新冠肺炎药物上市进程。
目前阿兹夫定在中国、俄罗斯、巴西开展的针对中重度新冠患者的III期临床试验已经完成,临床数据有待公布。目前真实生物已经向NMPA递交了阿兹夫定的新药上市申请(NDA),目前正处于审评审批阶段。根据国家药监局药审中心的信息披露,真实生物分别于今年3月10日、4月2日申请了II类和III类沟通交流会,当前状态为“已反馈”,目前公司正推进阿兹夫定治疗新冠肺炎药物上市进程。
阿兹夫定开始进行生产布局,合作企业或将获益
目前,真实生物已先后与新华制药、华润双鹤、奥翔药业等签订了针对阿兹夫定的委托生产协议,为获批上市后的商业化生产做足准备。此外,北京协和药厂和真实生物系阿兹夫定在国家药品监督管理局备案登记的生产厂家,真实生物拥有阿兹夫定的自主知识产权。
2022年4月26日,新华制药发布公告称与真实生物签署《战略合作协议》,基于真实生物致力于药品的研发和注册,并拥有阿兹夫定等产品的药品注册证书和/或专利权,以及相关有价值的和专有的信息和数据;新华制药拥有cGMP的药品生产能力,同意依照注册文件中规定的相关要求为真实生物生产相关产品,满足真实生物在中国及潜在的国际市场的注册和销售需求。真实生物同意新华制药为其在中国及经双方同意的其他国家的产品生产商和经销商,协议有效期十年。
2022年5月9日,华润双鹤发布公告称与真实生物在北京签署了《战略合作协议》及《阿兹夫定片委托加工生产框架协议》,就产品研发、产品生产以及市场推广达成战略合作协议,有效期为十年。目前华润双鹤已向北京市药品监督管理局提交药品生产许可证C证核发申请并获审批通过,具备受托加工该产品的生产能力和质量保证能力。后续将由真实生物向相关部门提交有关“增加生产地址”的药品生产许可证B证核发申请。双方根据阿兹夫定片开展临床试验、批准上市应用各阶段的实际情况,针对委托加工生产涉及的订单计划、结算方式、交货期限以及质量要求等具体事项,另行签署委托合同。委托加工框架协议涉及的阿兹夫定产品,其上市许可持有人为真实生物,华润双鹤仅为该产品的受托加工生产企业,不享有其所有权。
2022年5月10日,奥翔药业在股票交易异动公告中称其全资子公司浙江麒正药业有限公司日前已就阿兹夫定片的加工生产与真实生物签订了《委托加工生产框架协议》和《药品委托生产质量协议》。阿兹夫定的上市许可持有人为真实生物,麒正药业不享有其所有权,仅为受托加工生产企业,具体订单计划、结算方式、交货期限等需等到阿兹夫定获得批准后,再另行签署相应合同,双方能否最终签署相应合同以及签署的时间均存在不确定性。麒正药业相关片剂生产线尚须通过 GMP 符合性检查、取得药品生产许可证 C 证后,方可进行上市药品委托生产。
此外,2022年3月7日,拓新药业在回复交易所关注函中称其子公司新乡制药股份有限公司拥有阿兹夫定原料药的生产许可,真实生物拥有原料药下游阿兹夫定片的生产许可。截至公告发布时,新乡制药对正在进行的“阿兹夫定中间体新工艺及工业化”的研发已投入708万元,现有阿兹夫定原料药的产能、产量及销量均较小,最近一年一期实现的营业收入占公司营业收入的比例均在5%以下,收入及占比较低。根据5月26日发布的投资者关系活动记录表,阿兹夫定原料药新产线已经实现量产,生产计划一直在稳步快速推进中,目前产线的产能可以满足市场及客户的需要,未来将根据市场需求及订单情况,有序安排生产。
风险提示:
医改政策波动风险,市场竞争加剧风险,上游原材料涨价风险。


邓周宇,医药生物行业首席分析师、大消费组组长、11年医药行业研究经验,先后供职于、、中银国际证券。广泛覆盖:行业政策、创新药、医疗服务、医疗器械、医药流通业、中药行业、互联网医疗、商业健康险研究。曾获得:金融界最佳分析师(2013)、新财富最佳分析师(2014)、水晶球最佳分析师(2014、2017公募组,2021)、金牛奖最佳分析师(2014)、金翼奖最佳分析师(2017、2018)、万得金牌分析师(2014、2016)、网100强分析师(2021)。获上海财经大学经济学硕士学位。
邵子杭,加州大学伯克利分校生物工程硕士,并获得工程院奖学金。加州大学圣迭戈分校生物科学学士。长期积累实验室经验及项目管理经验。主要覆盖前沿医药板块,包括核酸疫苗、核酸药物、基因治疗、细胞治疗、抗体药物,同时覆盖血液制品。
周海涛,中国科学技术大学材料物理与化学硕士(学硕),香港中文大学(深圳)金融工程硕士。曾在中国科学院开展科学研究,并在国际核心期刊发表论文(一作)。累计近2年生物医药板块研究经历,主要覆盖医疗器械、IVD、CRMO、新兴AIDD、生物医药上游原材料等领域。
李天成,中山大学生物工程本科,导师为哈佛前讲师,国家青年千人教授;哥伦比亚大学生物医学工程研究生,导师为哥大医学院双院院士,《Biomaterials》主编。曾在国际核心期刊ACS Publication上发表论文,毕业后在美国药企工作近3年,曾就职于纳斯达克上市药企,负责药物的开发及测试。覆盖创新药&技术。
上一篇:国家为何不放开“新冠”管控
下一篇:走路不稳没劲,小脑萎缩共济失调怎么治疗?
最近更新热点资讯
- 谷歌AI聊天记录让网友San值狂掉:研究员走火入魔认为它已具备人格,被罚带薪休假
- 豆瓣9.4,姐弟恋、三人行,这部大尺度太厉害
- Genes, Intelligence, Racial Hygiene, Gen
- 【土耳其电影】《冬眠》电影评价: 宛如一部回归伯格曼风格的道德剧
- 陌生人社会伦理问题研究
- 理论研究|前海实践的价值理性和工具理性
- 澳门刑事证据禁止规则
- 综艺普及剧本杀和密室逃脱助力线下实体店爆发式增长
- 日本小伙和五个小姐姐同居?看完我酸了!
- 第一学期高一语文考试期中试卷
- 高中必考的物理公式有哪些
- 这部大尺度的申奥片,却讲述了不lun恋...
- 心理语言学论文精品(七篇)
- 《贵妃还乡》 超清
- 专论 | 郭丹彤、陈嘉琪:古代埃及书信中的玛阿特观念
- 微专业招生 | 数字文化传播微专业列车即将发车,沿途课程抢先看!
- 生态安全的重要性汇总十篇
- 原创因“18禁”电影登舆论顶峰,万千少女一场春梦:这一生,足够了
- 章鱼头
- 读书心得体会
- 考研考北京大学医学部或者协和是一种怎样的难度?
- 央媒评女主播编造“夜宿故宫”:让肇事者付出代价,理所应当
- 库欣病患者求医记(流水账)
- 《太平公主》④ | 地位越高,越要装傻
- 爱体检 安卓版 v2.5
