 手机访问:wap.265xx.com
手机访问:wap.265xx.com抗体药物研究新热点 l 双特异纳米抗体
? 双特异抗体
1997年第一个单克隆抗体药物被批准上市以来,肿瘤CAR-T治疗、中和抗体抗病毒疗法、免疫、代谢疾病治疗取得飞速发展,遗憾的是批准的单抗药物在进入临床单抗的比例正在逐年递减,抗体药物研发亟需转换方向。自1960年Nisonoff 及其合作者首次提出双特异抗体(BsAb)的概念,首个BsAb药物Catumaxomab于2009年被欧盟批准上市,给抗体药物研发领域带来曙光。发展至今,不同的双特异性抗体在实验室被成功构建,但由于VH和VL融合的错误产物比例过高应用于生产难度大,因此双特异抗体的研发仍具挖掘空间。
双特异纳米抗体
纳米抗体(Nanobody)是由比利时科学家于1993年在自然杂志中首次报道,只包含一重链可变区VHH,得益于小分子量(15KDa)、与人源VHs高度同源以及稳定性高等优势,近年来纳米抗体药物研究发展尤为迅速。为解决纳米抗体成药性的问题,纳米抗体工程改造集中在增加纳米抗体效价与在体内稳定性。通过基因工程、化学方法的改造,构建出多样的纳米抗体融合分子,例如融合了Fc的纳米抗体片段能够有效激活体内ADCC效应,融合人血清蛋白(HSA)能有效延长纳米抗体在体内的半衰期,从而改善药代动力学特征[2]。值得关注的是利用纳米抗体可以构建出的双特异性抗体分子,仍能够保持其组织渗透性,因此双特异纳米抗体在抗体工程研究领域具有非常广阔的前景[1],并且在与其他抗体片段或是与非抗体片段融合方式上,纳米抗体体现了更多样性的分子结构,设计出的多价多特异抗体联合分子,在肿瘤治疗、免疫疾病等领域也获得更好的效果[3]。
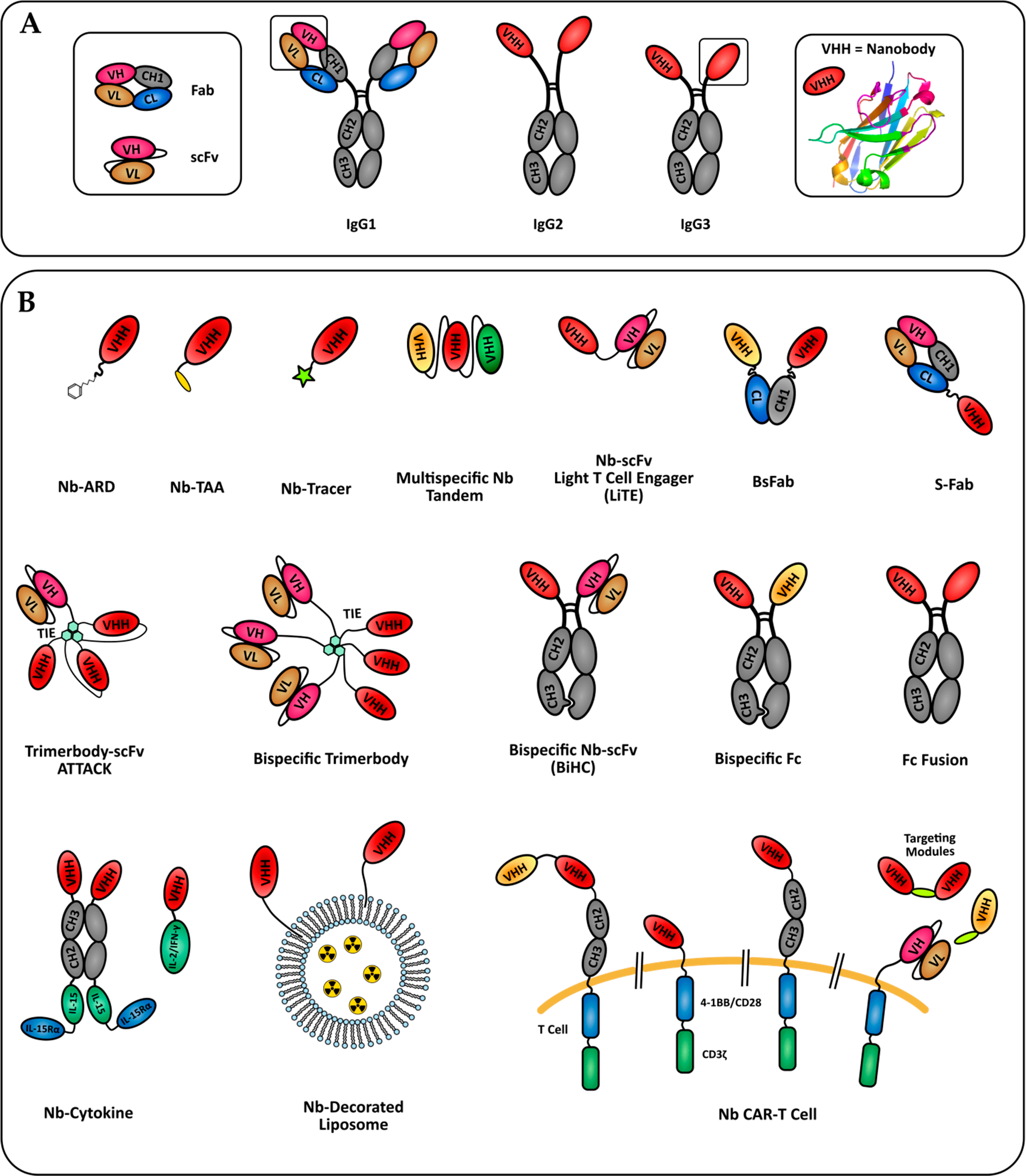
图 1 纳米抗体工程改造[1]
双特异性纳米抗体构建策略
1、VHH与VHH的融合
利用VHH hinge区序列或是Linker连接肽,连接两个以上纳米抗体分子,直接构建出双特异性纳米抗体。最小的双特异抗体(Tandem)由一段短肽将两个纳米抗体分子头尾相连,Zhimin Xu[4]利用(G4S)3构建出anti-EGFR/CD16/HSA双特异靶向重组纳米抗体,不仅延长了纳米抗体的半衰期,在体内具有抗肿瘤作用。Linlin Ma[5]等成功构建4价PD-L1/TIGIT双特异纳米抗体,相较于单价抗体具有更高的阻断活性。构建抗免疫球蛋白纳米抗体,同样能延长纳米抗体在体内的半衰期[6]。
2、VHH与其他抗体片段融合
VHH可与IgG1 的CH1和C?/Cλ片段融合,替代VH与VL片段,获得VHH-based 单价类IgG 双/三特异性抗体[7]。VHH与Fc融合的双特异抗体分子量大约80kDa,也远远小于全长IgG(~150kDa),使得其不仅具有IgG相同的功能效应,还具有更高的组织渗透性。VHH与Fab或ScFv组合,实现更多样性、高潜质的双特异抗体分子。
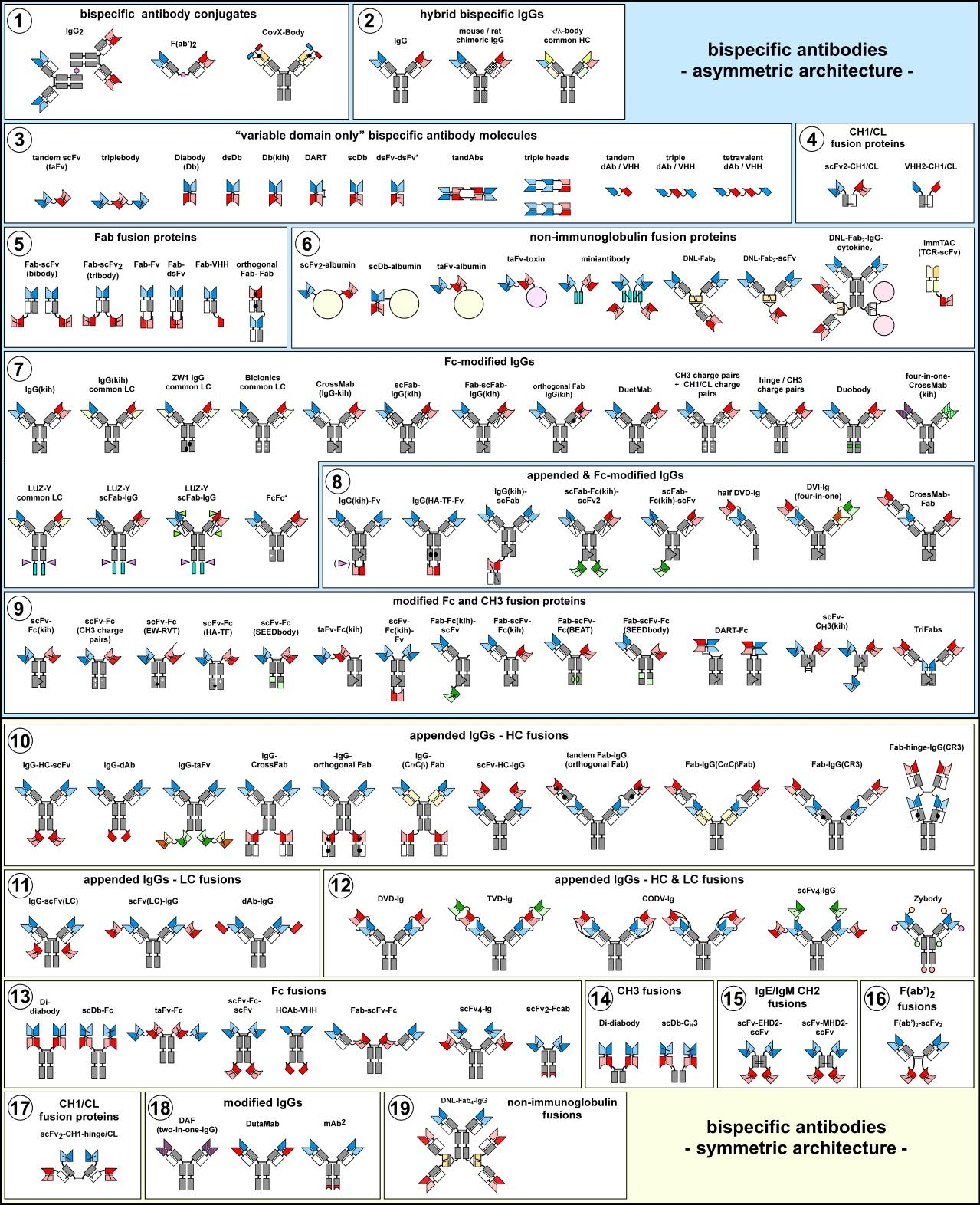
图 2 双特异抗体构建策略[9]
靶点研究
双特异抗体的研究主要靶向肿瘤环境抗原以及激活免疫活性,以PD-1/PD-L1与CTLA-4为代表肿瘤治疗方案的成功使得双特异抗体更加具有研究前景。安进公司设计的双抗T细胞激动剂(BiTEs)是抗体激活T细胞杀死肿瘤细胞的成熟技术,然而使用纳米抗体研发的类BiTEs分子会更小,高度模块化的纳米抗体也能适应多种肿瘤的治疗。一般来说,抗肿瘤双特异靶点研究主要集中在以下三个方向:
01
靶向免疫细胞:anti-CD3纳米抗体能够激活T细胞,anti-CD3融合抗肿瘤抗原的双抗纳米抗体,既具有CAR-T的效果,还降低了体内免疫反应。构建同时识别肿瘤细胞抗原与NK细胞表面受体CD 16a的双特异抗体可以增强体内ADCC效应[8]。
02 靶向肿瘤细胞抗原:通过抗体靶向肿瘤细胞受体,激活T细胞加强抗肿瘤疗效,EGFR、CD19、CEA、Her2都是近年来研究热门靶点。
03
靶向肿瘤环境:肿瘤细胞会在体内形成复杂的肿瘤微环境,尤其在实体瘤治疗中,免疫细胞很难进入肿瘤微环境,并且环境中的免疫细胞也会被抑制,靶向肿瘤环境抗体更适应临床实体瘤的治疗。
双特异抗体按照靶向分类有三种不同设计方案,一是单独靶向肿瘤细胞,二是单独靶向免疫细胞。但就目前双特异抗体研究来看,还没有靶向单独肿瘤细胞或是单独免疫细胞的成功案例,因此大部分研究都基于第三种设计方案,即肿瘤细胞和免疫细胞双靶向联合,激发靶向性免疫反应[10],例如利用anti-PD-1、anti-CTLA-4能够激活T细胞免疫应答,并且防止肿瘤的免疫逃逸。Pallavi Bhatta[11]等通过体外构建Fab-KD-Fab融合蛋白文库,高通量筛选成功构建了具有联合抑制B细胞活力作用的anti-CD79a/b和anti-CD22双特异抗体。
通过激活免疫细胞可以对抗肿瘤,相反通过抑制免疫应答可以治疗慢性炎症等免疫性疾病。OX40/XO40L是调节免疫检查点重要通路,XO40与XO40L结合能够促进T细胞增值并且抑制调节型T细胞作用[12],利用anti-OX40L阻断与配受体结合,能够抑制Th2细胞介导的免疫反应[13]。
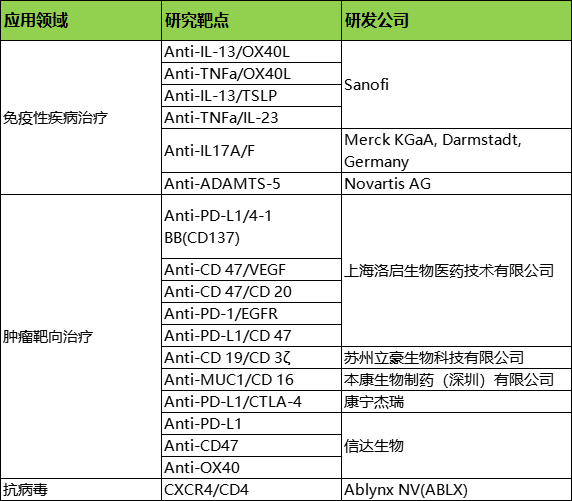
表 1 部分双特异纳米抗体专利靶点(公开资料)
? 总 结
纳米抗体的应用,远不止于肿瘤治疗,在免疫疾病治疗、抗体中和毒素领域均有优异的表现。另外相较于传统抗体,纳米抗体天然缺失轻链,极大简化了分离纯化步骤,进而提高了产品质量。双特异性纳米抗体兼具双特异性抗体与纳米抗体的双重优势,不仅具有更强的亲和力,延长了纳米抗体在体内的作用时间,并且在防止耐药、免疫逃逸方面都具有独特的优势。
????参考文献:
[1] Timothée Chanier, Patrick Chames. Nanobody Engineering: Toward Next Generation Immunotherapies and Immunoimaging of Cancer. Antibodies (Basel). 2019 Jan 21;8(1):13.
[2] Davé E, Adams R, Zaccheo O, et al. Fab-dsFv: A bispecific antibody format with extended serum half-life through albumin binding. MAbs. 2016 Oct;8(7):1319-1335.
[3] Coppieters K, Dreier T, Silence K, et al. Formatted anti-tumor necrosis factor alpha VHH proteins derived from camelids show superior potency and targeting to inflamed joints in a murine model of collagen-induced arthritis. Arthritis and Rheumatism, 2006, 54(6):1856-1866.
[4] Zhimin Xu, Chuangnan Qiu, Biyan Wen, et al. A bispecifific nanobody targeting the dimerization interface of epidermal growth factor receptor: Evidence for tumor suppressive actions in vitro and in vivo Biochemical and Biophysical Research Communications 548 (2021) 78-83.
[5] Linlin Ma, Junwei Gai, Peng Qiao, et al. A novel bispecific nanobody with PD-L1/TIGIT dual immune checkpoint blockade. Biochem Biophys Res Commun. 2020 Oct 15;531(2):144-151.
[6] M M Harmsen, H P D Fijten, A Dekker, P L Eblé. Passive immunization of pigs with bispecific llama single-domain antibody fragments against foot-and-mouth disease and porcine immunoglobulin. Vet Microbiol. 2008 Nov 25;132(1-2):56-64.
[7] Lukas Pekar, Michael Busch, Bernhard Valldorf, et al. Biophysical and biochemical characterization of a VHH-based IgG-like bi- and trispecific antibody platform. MAbs. Jan-Dec 2020;12(1):1812210.
[8] Yining Zhao,Yumei Li,Xiaoqiong Wu, et al. Identification of anti-CD16a single domain antibodies and their application in bispecific antibodies, Cancer. Biology. Therapy. 21(2020) 72-80
[9] Brinkmann U, Kontermann RE. The making of bispecific antibodies. MAbs. 2017 Feb/Mar;9(2):182-212.
[10] Frans V. Suurs , Marjolijn N. Lub-de Hooge , ElisabethG.E. de Vries, Derk Jan A. de Groot. A review of bispecific antibodies and antibody constructs in oncology and clinical challenges. Pharmacol Ther. 2019, S0163-7258(19)30069-5.
[11] Pallavi Bhatta, Kevin D. Whale, Amy K. Sawtell, et al. Bispecific antibody target pair discovery by highthroughput phenotypic screening using in vitro combinatorial Fab libraries. Mabs. 2021, VOL. 13, NO. 1, e1859049.
[12] Deng J, Zhao S, Zhang X, et al. OX40 (CD134) and OX40 ligand, important immune checkpoints in cancer. Onco Targets Ther. 2019;12:7347-7353.
[13] Wang YH, Liu YJ. OX40-OX40L interactions: a promising therapeutic target for allergic diseases? J Clin Invest. 2007 Dec;117(12):3655-7.
上一篇:上海科学家最新发现:奥密克戎感染力是野生型的近十倍
下一篇:肝病患者如何选用退烧药物?专家:对症治疗,尽量少吃药
最近更新热点资讯
- 谷歌AI聊天记录让网友San值狂掉:研究员走火入魔认为它已具备人格,被罚带薪休假
- 豆瓣9.4,姐弟恋、三人行,这部大尺度太厉害
- Genes, Intelligence, Racial Hygiene, Gen
- 【土耳其电影】《冬眠》电影评价: 宛如一部回归伯格曼风格的道德剧
- 陌生人社会伦理问题研究
- 理论研究|前海实践的价值理性和工具理性
- 澳门刑事证据禁止规则
- 综艺普及剧本杀和密室逃脱助力线下实体店爆发式增长
- 日本小伙和五个小姐姐同居?看完我酸了!
- 第一学期高一语文考试期中试卷
- 高中必考的物理公式有哪些
- 这部大尺度的申奥片,却讲述了不lun恋...
- 心理语言学论文精品(七篇)
- 《贵妃还乡》 超清
- 专论 | 郭丹彤、陈嘉琪:古代埃及书信中的玛阿特观念
- 微专业招生 | 数字文化传播微专业列车即将发车,沿途课程抢先看!
- 生态安全的重要性汇总十篇
- 原创因“18禁”电影登舆论顶峰,万千少女一场春梦:这一生,足够了
- 章鱼头
- 读书心得体会
- 考研考北京大学医学部或者协和是一种怎样的难度?
- 央媒评女主播编造“夜宿故宫”:让肇事者付出代价,理所应当
- 库欣病患者求医记(流水账)
- 《太平公主》④ | 地位越高,越要装傻
- 爱体检 安卓版 v2.5
